唯一器械标识(Unique Device Identification,缩写UDI)是美国FDA建立的”特殊医疗器械的识别系统”。
UDI是医疗器械在产品供应链中的唯一的“身份ID”,是对医疗器械在其整个生命周期赋予的身份标识,具有唯一性和可追溯性。
目前,欧美、日韩等发达国家都已经制定成熟的UDI政策法规,强制要求在本国销售、流通的医疗器械上必须实施UDI标识。
1、UDI的生命周期
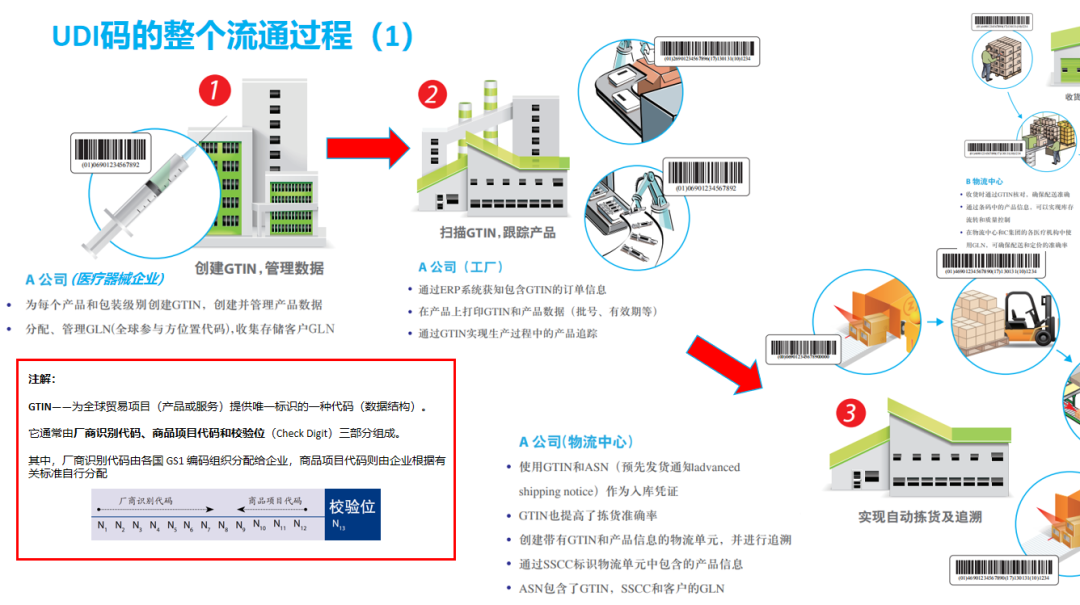
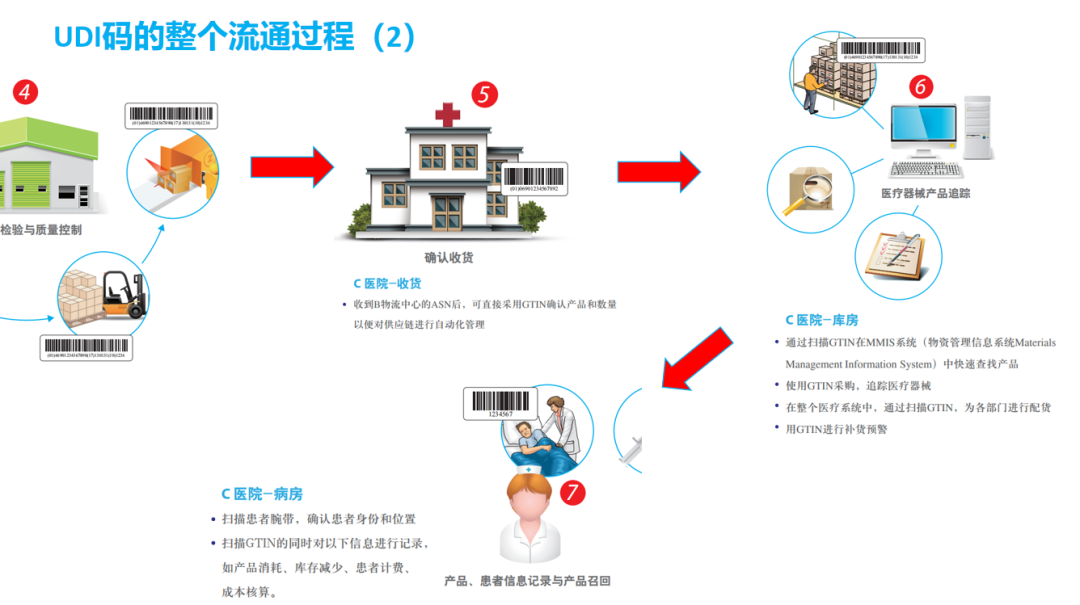
2020年10月1日起,第一批实施UDI的医疗器械企业,所有销售产品必须具有UDI标识,否则不得上市。
2、全球UDI标识工作进程


3、医疗器械UDI标识的应用范围

第一批需要实现UDI管控的医疗器械有9大类器械,分别包含:
01 有源手术器械
02 无源手术器械
03 神经和心血管手术器械
06 医用成像器械
10 输血、透析和体外循环器械
12 有源植入器械
13 无源植入器械
14 注输、护理和防护器械
16 眼科器械
4、UDI标识的结构组成、编码机构、数据库
UDI标识组成:器械识别码(DI)+ 生产识别码(PI)
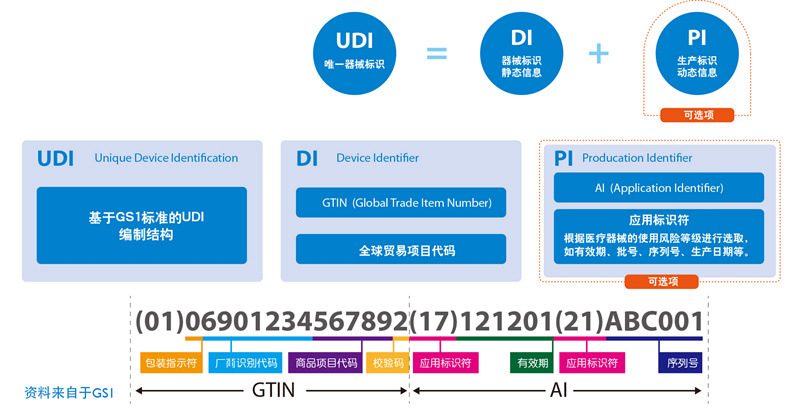
目前全球认可的UDI编码机构及其编码方式有以下5种:
5、UDI标签的载体、样式及特点
目前UDI唯一标识的数据载体主要有:一维条码、二维条码和射频标签(RFID)三种形式。
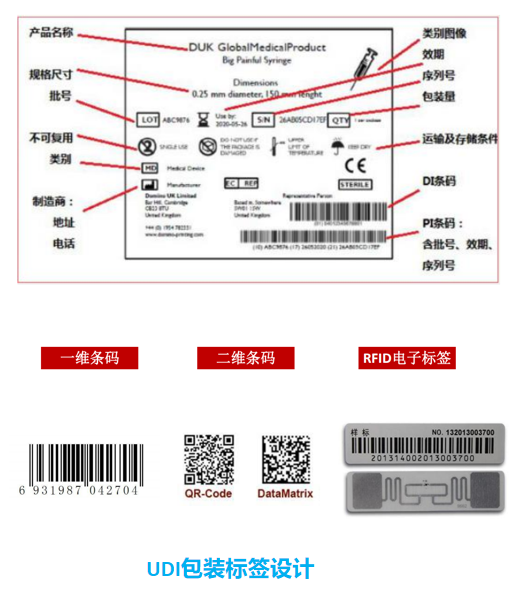
UDI标识必须满足可识别和可数据采集的要求。
6、一站式UDI标识解决方案
安田科技为医疗器械企业的UDI标识需求提供完整的一站式解决方案。

针对不同的医疗器械包装材质、产品特点配备不同的安田科技标识产品搭建可行的UDI管理系统,对接各方数据平台。
安田科技可为众多医疗器械生产企业,提供一站式UDI标识解决方案,助力企业管控。
服务热线:0571-86716693!
















